
流式实验必备!常见单细胞悬液制备操作步骤(上)
发表时间:2025-03-18众所周知,成功的实验往往依赖于高质量的样本制备,而对于流式细胞术来说,单细胞悬液的制备是实验顺利进行的关键。为了进行有效的流式分析,必须将组织分散成单个细胞,并保持细胞的基本属性和生物学特性。因此,在流式实验中,如何制备出合格且分散均匀的单细胞悬液,成为了样本制备的核心要点。今天将为大家介绍几种常见的组织样本单细胞悬液制备方法,帮助大家在流式细胞术实验中取得更好的结果。
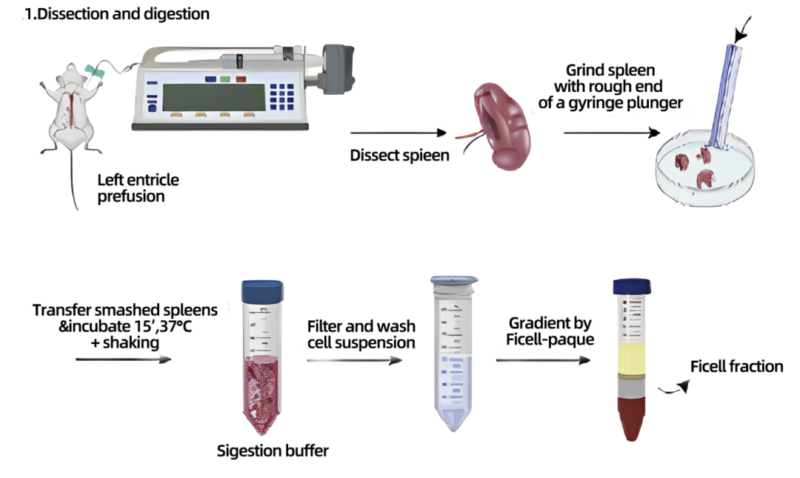
一、脾脏单细胞悬液制备操作步骤
1.将切除的脾脏组织剪成小块。
2.将碎片放置在连接到50 mL圆锥管的筛网上。
3.使用注射器活塞轻轻挤压脾脏碎片,通过筛网进行细胞分离。
4.用过量的PBS缓冲液冲洗,帮助细胞通过筛网。
5.以1,600 rpm的速度离心细胞悬液5分钟,收集细胞沉淀。
6.小心吸取上清液。
7.将细胞沉淀重新悬浮在2 mL预热至37°C的红细胞裂解液中。
8.在37°C水浴中孵育细胞2分钟。
9.加入至少30 mL的PBS,重复以1,600 rpm离心5分钟。
10.丢弃上清液后,将细胞重新悬浮在PBS中,最终浓度调整为每毫升2 x 10^6个细胞。
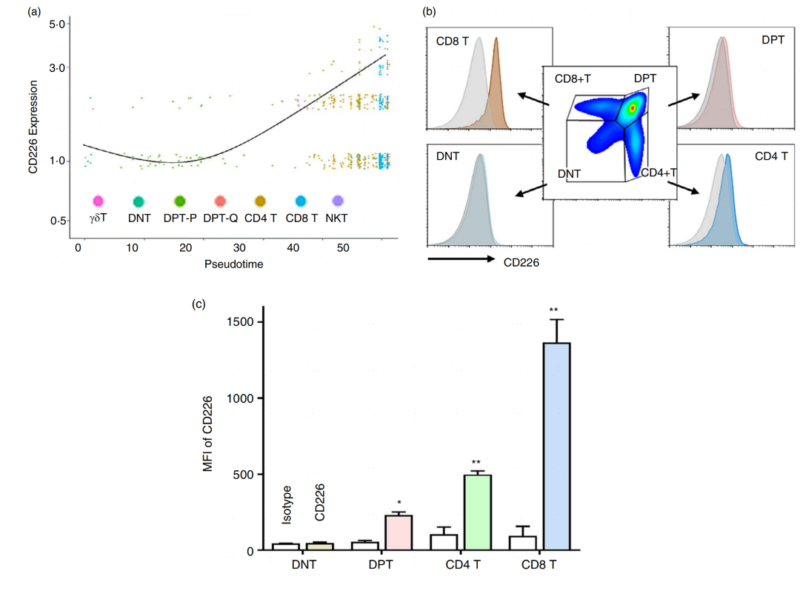
二、胸腺单细胞悬液制备操作步骤
(Ⅰ)将胸腺取出并置于无菌PBS溶液中浸泡。
(Ⅱ)将胸腺组织放入200目筛网中,使用组织研磨棒轻轻研磨,直到没有明显的块状物。
(Ⅲ)用15 mL PBS缓冲液冲洗筛网,将冲洗液收集到15 mL离心管中,进行300 g离心5分钟,弃去上清液。
(Ⅳ)用细胞染色缓冲液重悬胸腺细胞并计数,将细胞浓度调整至1×10^7个/mL。
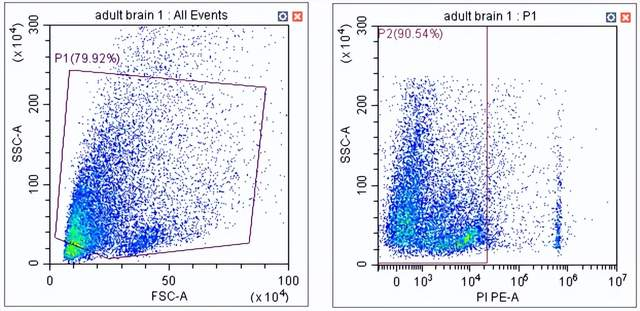
三、脑组织单细胞悬液制备操作步骤
小鼠脑组织单细胞悬液的制备方法有多种,常见的包括酶解消化法、组织解离器法和研磨法。首先,使用含胶原酶Ⅳ和DNase I的消化液,鼠脑分割后与消化液混合,常见的处理方式包括:
(1)酶解消化+摇床:将鼠脑用钝性镊子分割后放入消化液中,放置于37℃摇床震荡2小时。
(2)酶解消化+组织解离器:在消化液中处理鼠脑后,使用组织解离器进行震荡,约2分钟后观察脑组织解离成乳糜状。
(3)Trypsin消化+组织解离器:使用Trypsin消化液处理,结合组织解离器加热至37℃进行缓慢震荡,通常约30分钟。
(4)研磨杵研磨:将鼠脑分割后放入研磨玻璃中,加入消化液,用玻璃研磨棒反复按压直至完全解离,避免产生气泡影响细胞活性。
流式细胞术分析依赖于单细胞水平的精确测量,因此在处理不同组织时,必须选择对细胞损伤最小、产率较高的单细胞悬液制备方法。这能最大限度地保持细胞的原始特性,从而确保实验结果的准确性和可靠性。js33333金沙线路检测依托其先进的单克隆抗体开发平台,提供高亲和力和高特异性的经典克隆细胞株纯化抗体,广泛应用于多种免疫细胞亚群的检测,包括但不限于Th细胞。这些抗体涵盖人类、大鼠、小鼠等多个物种,提供丰富的检测指标选择。此外,js33333金沙线路检测还为客户提供免费的颜色搭配建议、实验操作指导及数据分析服务,致力于为客户提供全面的流式细胞术解决方案。
以下是推荐的流式抗体配方方案,用于检测不同免疫细胞亚群
| 流式抗体推荐 | |||
| 种属 | 细胞群 | 流式抗体搭配 | 货号 |
| Human | T/B/NK细胞群检测 | CD45-PerCP | PCP-30039 |
| CD3-FITC | FITC-30004 | ||
| CD16-PE | PE-30061 | ||
| CD56-PE | PE-30008 | ||
| CD19-APC | APC-30066 | ||
| Human | Th1/Th2 细胞群检测 | CD3-PerCP/Cyanine5.5 | PCP55-30004 |
| CD4-FITC | FITC-30005 | ||
| IFN-γ-PE | PE-30053 | ||
| IL4-APC | APC-30043 | ||
| Mouse | Th1/Th2 细胞群检测 | CD3-PerCP/Cyanine5.5 | PCP55-30002 |
| CD4-FITC | FITC-30001 | ||
| IFN-γ-PE | PE-30074 | ||
| IL4-APC | APC-30026 | ||
| Human | Treg细胞群检测 | CD4-FITC | FITC-30005 |
| CD25-PE | PE-30035 | ||
| CD127-APC | APC-30033 | ||
| Mouse | Treg细胞群检测 | CD4-FITC | FITC-30001 |
| CD25-PE | PE-30017 | ||
| FOXP3-APC | APC-30055 | ||

 联系我们
CONTACT
联系我们
CONTACT


